Kontakt:Errol Zhou (Pán.)
Tel: plus 86-551-65523315
Mobil/WhatsApp: plus 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Email:sales@homesunshinepharma.com
Pridať:1002, Huanmao Budova, č.105, Mengcheng Cesta, Hefei Mesto, 230061, Čína
Spoločnosti Pfizer (Pfizer) a Myovant Sciences nedávno oznámili, že podali dávky prvému predmetu v štúdii SERENE fázy 3. Štúdia hodnotí antikoncepčný účinok tabliet zlúčeniny relugolixu (relugolix 40 mg, estradiol 1, 0 mg, norethindrone acetát 0, 5 mg) u zdravých žien vo veku 18- 35 rokov, u ktorých je riziko gravidity. Relugolix je antagonista receptora perorálneho gonadotropínu uvoľňujúceho hormón (GnRH). V súčasnosti novú aplikáciu lieku (NDA) zlúčenín relugolixu na liečbu ženských myómov maternice skúma americký FDA a očakáva sa, že 1. Okrem toho spoločnosti Pfizer a Myovant plánujú v prvej polovici roka 2021 predložiť novú žiadosť o liek na tablety zlúčeniny relugolixu na liečbu stredne ťažkej až silnej bolesti súvisiacej s endometriózou.
Juan Camilo Arjona Ferreira, MD, hlavný lekár myovantných vied, povedal: "Zaviazali sme sa predefinovať starostlivosť o ženy, čo znamená podporovať ich celkové zdravie a kvalitu života. Mnoho ľudí s myómami maternice a endometriózou Ženy musia kontrolovať svoje príznaky a reprodukčné možnosti, vrátane prevencie tehotenstva. Cieľom štúdie SERENE fázy 3 je vyhodnotiť potenciál tabliet zlúčeniny relugolixu na prevenciu gravidity a doplní údaje z našich projektov FÁZY 3 LIBERTY a SPIRIT, ktoré potvrdili tablety zlúčeniny relugolixu Prospects ako potenciálnu liečbu myómov maternice a endometriózy."
Štúdia SERENE prijme 900 sexuálne aktívnych zdravých žien vo veku 18 - 35 rokov s normálnou plodnosťou. Primárnym koncovým ukazovateľom účinnosti je Pearlov index (Pearl Index), ktorý je definovaný ako počet gravidných žien na liečbu na 100 žien, ktoré používajú určitú antikoncepčnú metódu počas 1 roka. Tehotenstvo počas liečby sa vzťahuje na tehotenstvo od odhadovaného dátumu tehotenstva v prvý deň študijného zákroku do siedmich dní (vrátane siedmeho dňa) po podaní posledného skúmanej drogy. Ženy budú dostávať tablety zlúčeniny relugolixu raz denne počas 13 vysokorizikových cyklov po 28 dňoch. Počas štúdie sa budú zhromažďovať aj údaje o bezpečnosti.
V apríli 2020 myovant oznámil výsledky jednoramožkovej, otvorenej štúdie supresie ovulácie fázy 1, ktorej cieľom je vyhodnotiť účinok tabliet zlúčeniny relugolixu na supresiu ovulácie na základe hodnotiacej škály Hoogland- Skouby (skóre<5). in="" 67="" healthy="" women,="" after="" 84="" days="" of="" treatment="" (3="" cycles),="" relugolix="" compound="" tablets="" treatment="" achieved="" 100%="" ovulation="" suppression,="" and="" the="" overall="" tolerance="" was="" good.="" in="" addition,="" 100%="" of="" women="" resume="" ovulation="" or="" menstruation="" after="" stopping="" treatment,="" and="" the="" average="" ovulation="" time="" is="" 23.5="" days.="" the="" data="" of="" this="" study="" was="" published="" at="" the="" 2020="" virtual="" conference="" of="" the="" american="" society="" of="" reproductive="" medicine="">
Pfizer Global Product Development Senior Viceprezident a chief Development Officer James Rusnak, MD, povedal: "Výsledky štúdie fázy 1 ukazujú, že tablety zlúčeniny relugolixu inhibujú ovuláciu u všetkých účastníkov štúdie a poskytujú základ pre štúdiu SERENE na vyhodnotenie tabliet zlúčeniny relugolixu. Či existuje potenciál zabrániť otehotneniu u žien podstupujúcich liečbu. Údaje z tejto štúdie fázy 3 poskytnú dôležité informácie pre rozhodnutia o liečbe žien s endometriózou a myómami maternice."
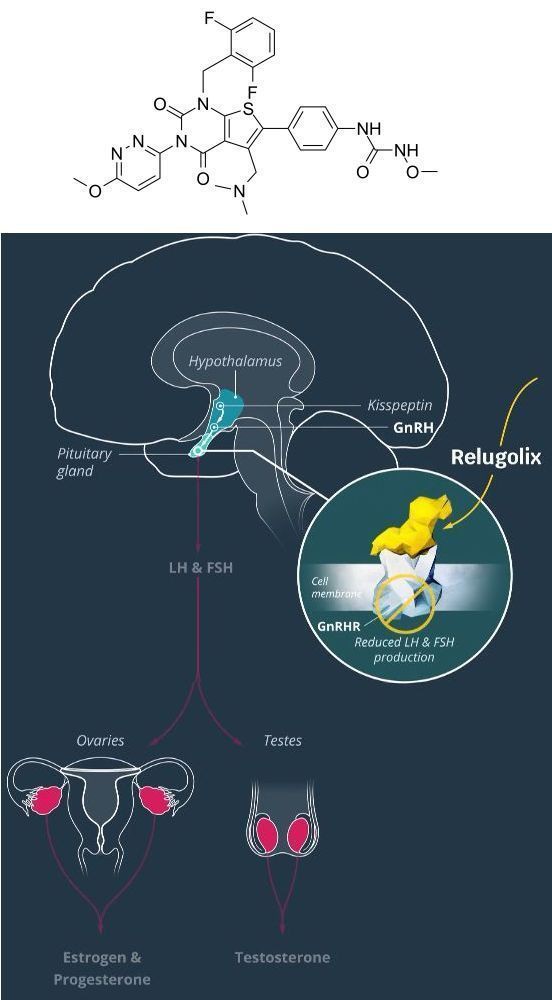
Chemická štruktúra a mechanizmus účinku Relugolix (zdroj štrukturálneho vzorca: medchemexpress.com)
V decembri 2020 dosiahli spoločnosti Pfizer a Myovant Sciences dohodu o spolupráci vo výške 4,2 miliardy USD na vývoj a komercializáciu relugolixu v Spojených štátoch a Kanade v oblasti onkológie a zdravia žien. Spoločnosť Pfizer tiež získa výhradné právo komercializovať relugolix na onkológiu mimo Spojených štátov a Kanady (okrem určitých ázijských krajín).
Relugolix je antagonista receptora perorálneho hormónu uvoľňujúceho gonadotropín (GnRH), ktorý inhibuje produkciu testosterónu v semenníkoch, hormónu, ktorý stimuluje rast rakovinových buniek prostaty. Okrem toho môže relugolix tiež znížiť produkciu ovariálneho estradiolu blokovaním receptorov GnRH v hypofýzy. Je známe, že tento hormón stimuluje rast myómov maternice a endometriózy.
relugolix bol vyvinutý spoločnosťou Takeda a Myovant Sciences (spoločnosť založená spoločnosťou Roivant a Takeda) získala exkluzívnu globálnu licenciu v júni 2016 s výnimkou Japonska a ďalších ázijských krajín. V Japonsku bol relugolix schválený v januári 2019 a uvádzaný na trh pod značkou Relumina na zlepšenie nasledujúcich príznakov spôsobených myómami maternice: menorágia, bolesť v dolnej časti brucha, bolesť dolnej časti chrbta a anémia.
V súčasnosti myovant vyvíja perorálne tablety relugolixu (120 mg) raz denne na liečbu pokročilého karcinómu prostaty. 18. decembra 2020 bol Orgovyx (relugolix, 120 mg tablety) schválený americkou FDA na liečbu dospelých pacientov s pokročilým karcinómom prostaty.
Stojí za zmienku, že Orgovyx je prvý a jediný perorálny antagonista receptora GnRH schválený americkou FDA na liečbu pokročilého karcinómu prostaty. Liek bol schválený prostredníctvom procesu prioritného preskúmania. V štúdii HERO fázy 3 bola miera remisie pri liečbe relugolixom až 96, 7%, čo bolo signifikantne lepšie ako leuprolid acetát (88, 8%), pričom sa riziko závažných kardiovaskulárnych nežiaducich účinkov (MACE) znížilo o 54%.
Okrem toho, Myovant je tiež vývoj perorálne relugolix zlúčenina tablety (relugolix 40mg, estradiol 1. 0mg, norethindrone acetát 0, 5mg) raz denne na liečbu ženských myómov maternice a endometriózy. V súčasnosti americké FDA skúma tablety zlúčeniny relugolixu na liečbu ženských myómov maternice. Cieľovým dátumom činnosti je 1. Očakáva sa, že tablety zlúčeniny Relugolix na liečbu rakoviny endometria predložia v prvej polovici roka 2021 novej žiadosti o liek americkému FDA.